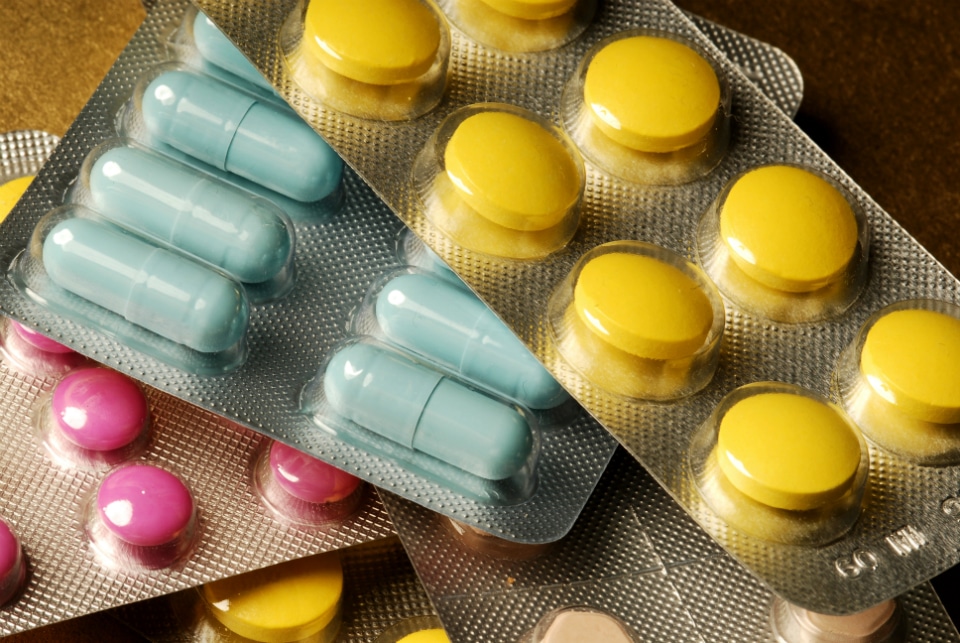
Un chiffre frappe d’emblée : plus de 70% des doses de médicaments consommées chaque jour en Italie proviennent de produits dont le brevet est tombé. Autrement dit, des médicaments génériques, ces copies officielles de traitements « de marque », qui débarquent sur le marché une fois la protection du brevet levée. Malgré une pénétration du marché encore timide comparée à d’autres pays européens, leur usage s’impose peu à peu, et même l’Italie s’y met sérieusement, comme le révèle le dernier rapport sur l’utilisation des médicaments.
Les génériques n’ont rien d’une nouveauté. Leur présence, déjà bien ancrée depuis plusieurs années, a permis au Service national de santé d’économiser plus d’un milliard et demi d’euros en six ans. Pourtant, c’est seulement à partir de 2013 que les résistances, longtemps tenaces, ont commencé à s’effriter dans le pays. Les mentalités évoluent, la méfiance recule, et ces médicaments trouvent enfin leur place dans les pharmacies et les habitudes.
A lire en complément : Pourquoi acheter un distributeur de médicament journalier ?
Mais qu’est-ce qu’un médicament générique, concrètement ? Peut-on s’y fier ? Qu’est-ce qui explique leur prix plus doux ? Voici de quoi y voir clair sur leur fonctionnement, leurs garanties et leur impact sur le système de santé.
Quand un médicament devient-il générique ? Un médicament générique n’est rien d’autre que la réplique d’un médicament déjà commercialisé, une fois la période de brevet arrivée à expiration. Ce brevet, véritable bouclier pour l’inventeur, interdit toute imitation pendant vingt ans à compter du dépôt de la demande, une règle valable aussi bien pour les médicaments que pour d’autres inventions.
A voir aussi : Ce qu'il faut vraiment savoir sur les médicaments périmés et leur danger
En pratique, le générique devient l’alternative directe au médicament « de marque », celui que le laboratoire a baptisé d’un nom commercial, parfois évocateur ou rassurant. Le générique, lui, n’a pas ce luxe : il ne peut être désigné que par le nom de sa substance active, c’est-à-dire la molécule qui agit réellement pour soigner ou soulager.
Pour illustrer, prenons le cas du paracétamol. Cette molécule, connue pour ses propriétés antalgiques et antipyrétiques, se retrouve à la fois dans des spécialités comme la Tachipirina et dans des génériques étiquetés simplement « paracétamol ».
Quelles exigences pour un médicament générique ? Pour être mis sur le marché, un médicament générique doit prouver sa bioéquivalence avec la spécialité de référence. Cela signifie qu’à dose et mode d’administration identiques, il doit délivrer la même quantité de principe actif dans l’organisme, au même rythme. Le profil de concentration dans le sang doit correspondre à celui du médicament original.
En clair, le générique doit contenir le même principe actif, à la même dose, respecter les mêmes indications thérapeutiques, se présenter sous la même forme pharmaceutique (comprimé, sirop, injection…) et emprunter la même voie d’administration. Seule nuance : les excipients, ces substances qui servent de support ou stabilisent la formulation, peuvent différer du médicament de marque, tant que la bioéquivalence reste garantie. Il s’agit par exemple de liants, conservateurs, colorants ou correcteurs de goût.
Les fabricants de génériques sont soumis aux mêmes standards de qualité que ceux qui produisent les spécialités. Le principe actif doit présenter un niveau de pureté identique, la stabilité du médicament final doit être démontrée, et l’emballage doit protéger le produit de façon adéquate.
Lorsqu’un générique coche toutes ces cases, il n’y a pratiquement aucune raison qu’il affiche des différences notables en matière d’efficacité ou de sécurité par rapport à la spécialité originale.
Qu’en est-il de la sécurité ? Les génériques doivent démontrer qu’ils ne présentent aucun risque pour la santé, exactement comme tout autre médicament. Avant d’arriver sur le marché, leur composition est évaluée pour garantir une utilisation sans danger dans la pratique médicale quotidienne.
Mais alors, pourquoi ne pas refaire tous les tests, comme pour un nouveau produit ? Tout simplement parce que le principe actif et les excipients ont déjà fait leurs preuves, parfois depuis des décennies. Reprendre les études animales et les essais de toxicité serait non seulement superflu, mais aussi contraire à l’éthique : inutile de répéter ce qui a déjà été validé, d’autant plus que cela impliquerait de nouveaux sacrifices d’animaux sans bénéfice réel.
La procédure de mise sur le marché se base donc sur la documentation existante et des rapports bibliographiques complets, ce qui suffit à garantir la sécurité du générique.
Générique ou équivalent : quelle différence ? La réalité, c’est que les deux termes désignent la même chose. Depuis 1995, « médicament générique » est la traduction française de « generic drug » utilisé dans les pays anglo-saxons. Mais pour dissiper les doutes, certains redoutaient que « générique » ne sonne comme « moins bon »,, l’appellation « médicament équivalent » a été introduite en 2005, afin d’insister sur la bioéquivalence avec la spécialité de référence. Aujourd’hui, les deux expressions circulent librement et renvoient au même concept.
Pourquoi les médicaments génériques sont-ils moins chers ? En Italie, la loi impose que le prix d’un générique soit inférieur d’au moins 20 % à celui du médicament original. Un coup de pouce notable pour le porte-monnaie des patients, mais aussi pour les finances publiques lorsque le médicament est remboursé.
Ce tarif plus bas s’explique aussi par la structure des coûts. Les entreprises qui fabriquent des génériques n’ont pas à financer la découverte de nouvelles molécules ni les longues études de toxicité et d’efficacité. Pas d’essais cliniques à grande échelle, mais uniquement des tests de bioéquivalence : le processus est plus rapide, moins onéreux, et les économies se répercutent directement sur le prix final.
Qui donne le feu vert ? Tous les médicaments commercialisés en Italie sont approuvés par l’Agence Italienne des Médicaments (Aifa). Les exigences pour décrocher l’Autorisation de Mise sur le Marché (AIC) sont identiques pour les génériques et les spécialités. La différence ? La procédure est plus rapide, car elle ne requiert pas de nouvelles études d’innocuité et d’efficacité.
Un générique n’est jamais une contrefaçon Il faut être clair : un médicament générique n’a rien à voir avec un médicament contrefait. Une contrefaçon désigne un produit frauduleusement étiqueté, dont la composition ou la provenance a été falsifiée. Ce phénomène concerne aussi bien les spécialités que les génériques, mais il s’agit d’une infraction grave, poursuivie par la loi.
En définitive, le générique s’impose comme une alternative fiable, règlementée et économique, loin des idées reçues. Si demain, en pharmacie, on vous propose un équivalent, vous saurez désormais ce qui se cache derrière ce nom : un médicament qui a déjà fait ses preuves, et qui, en silence, allège la facture de tous.